Spark はCresset社の生物学的等価体(Bioisostere)置換およびスキャフォールドホッピングツールですが、新たにドッキング機能が搭載されました。本事例紹介では、GSK-3βの活性部位の構造をもとに、Sparkを利用してリガンド-蛋白質相互作用を作ることのできる代替置換基を直接見つけ、それら置換基をランクづけすることを解説します。
はじめに
GSK-3βは、さまざまな細胞プロセスに関与するセリン/スレオニンキナーゼです。特に、成人の脳の中に広く存在することから、ニューロンのシグナル伝達経路での重要な役割が示唆されます。 GSK-3βは、躁鬱双極性障害、うつ病、統合失調症などの気分障害にも関連しており、その治療への期待からGSK-3β阻害薬の開発が活発に行われています。
1H-インダゾール-3-カルボキサミドは、近年発見されたATP競合性GSK-3β阻害薬の新しい構造クラスです1,2。Cmpd 1 (図1-左および表1) は、好ましいキナーゼ選択性プロファイルを示し、GSK-3βに対して細胞アッセイでも阻害活性が高く、躁病の動物モデルでは薬物動態特性とその有効性を確認されています。しかしながら、この化合物は甚大なhERG阻害を引き起こしてしまいます。
hERG阻害回避のために、Cmpd1を出発として、塩基性を下げる目的で(2-メトキシエチル)-4-メチルピペリジン部位をオキサニル基に置換し、親油性を下げるために極性のより高いジフルオロフェニル基を導入し、より高いGSK-3β阻害活性をもち、hERG阻害を回避するCmpd 14 (図1-右および表1) が見いだされました2。
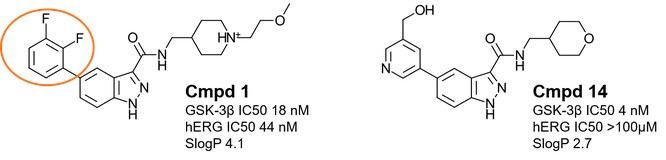
図1. Cmpd1(左): GSK-3β阻害活性は高いがhERG阻害を引き起こす Cmpd 14(右): 最適化によってGSK-3β阻害活性を高めhERG阻害を回避
Cmpd1の類縁体について詳細に検討されたSARデータを表1に示します。
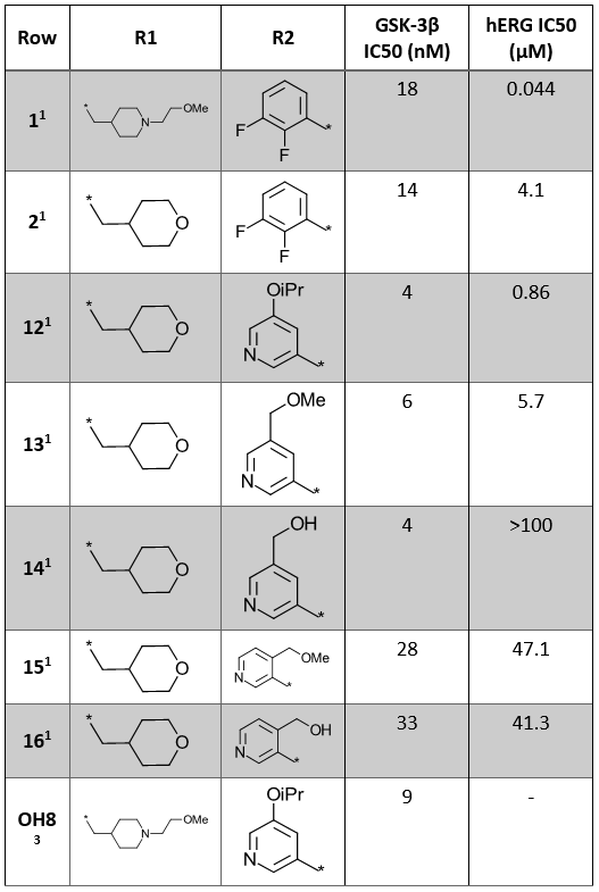
表1.1H-インダゾール-3-カルボキサミドコアのR1およびR2位置のSAR探索1,3
ここでは、Sparkの「ドッキング」機能を使用して、ジフルオロフェニル基に対する置換R-基を迅速に見つけ出します(図1橙円-左)。 この方法を利用すると、標的タンパク質のポケットの中の空隙にリガンドおよびフラグメントを成長させ、タンパク質の活性部位との相互作用を維持しながら、出発分子またはレファレンス分子と部分構造を異にする新規化合物を創出することができます。具体的には、GSK-3β活性部位と直接相互作用して活性を高めると同時に、親油性を下げてhERG阻害を低減する代替R-グループを探索しています。
タンパク質-リガンド複合体
Sparkでドッキングするためには、精密に準備されたタンパク質構造(水素原子の復元、内部水素結合ネットワークの最適化、衝突の回避、適切なプロトン化状態)を使って実験を行うことが必要です。Cmpd1がバインドしたGSK-3βとの複合体(PDB: 6TCU)の構造準備には、Cresset社のSBDDプラットフォームである Flare™ を利用しました。
このタンパク質-リガンドの構造では、インダゾールカルボキサミドがAsp133のカルボニル基、Val135のNHおよびカルボニルとの3つの水素結合によってGSK-3βのヒンジ領域と相互作用していることがわかります(図2)。 ピペリジン部分は溶媒側に飛び出していますが、ジフルオロフェニル基の環は触媒作用中心のLys85の近くに位置しています。
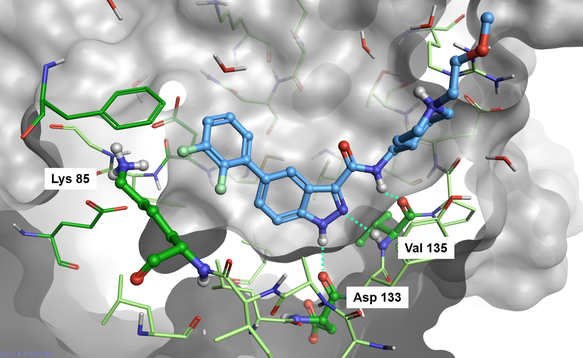
図2. GSK-3β活性部位にバインドしたCmpd1 (PDB: 6TCU)
Sparkでのドッキング
Sparkのドッキングワークフローは、まず出発分子の置換部分を削除することから始めます(図3、A-B)。次に、一部を切り取られた出発分子に新しいフラグメントを加え、Cresset XED力場によって計算されるタンパク質の静電場に従ってその活性部位に適切に配置します(図3、C)。そしてLeadFinder™の「スコアリング」ドッキングモードにより、新しい結果分子のポーズを最適化します(図3、D)。最後に、既知のリガンドの結晶学的ポーズを正しく評価するよう最適化されたLeadFinderの「ランク」スコアリング関数を使用して、得られた複数のポーズを序列化します (負のスコアがよい)。
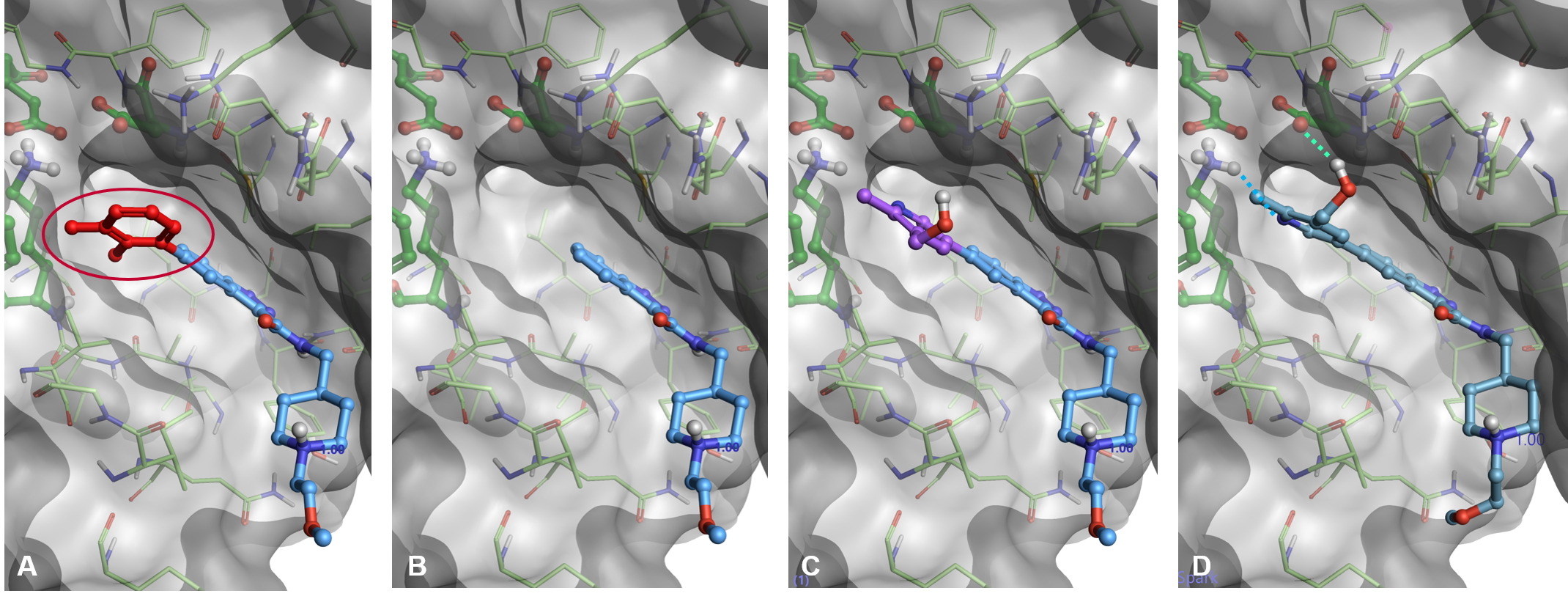
図3. Sparkでのドッキングワークフロー A) 出発分子の置換部分の選択 B) 選択フラグメントの削除 C) 新しいフラグメントポケットの中で適切に結合 D) 新規結果分子をLeadFinderで最適化
ここでは、簡単な手順に従うだけで適切な実験を準備できる「Scaffold Hopping or R-group Replacement」ウィザード(図4-左)を活用します。6TCUのタンパク質-リガンド複合体はFlareで最適化され、既にプロトン化された状態でSparkに読み込み、出発分子としてCmpd 1を選択し、全ての結晶学的水分子を除去します。そして、出発分子の置換領域としてジ-フルオロフェニル基部分を選択します(図4-右)。
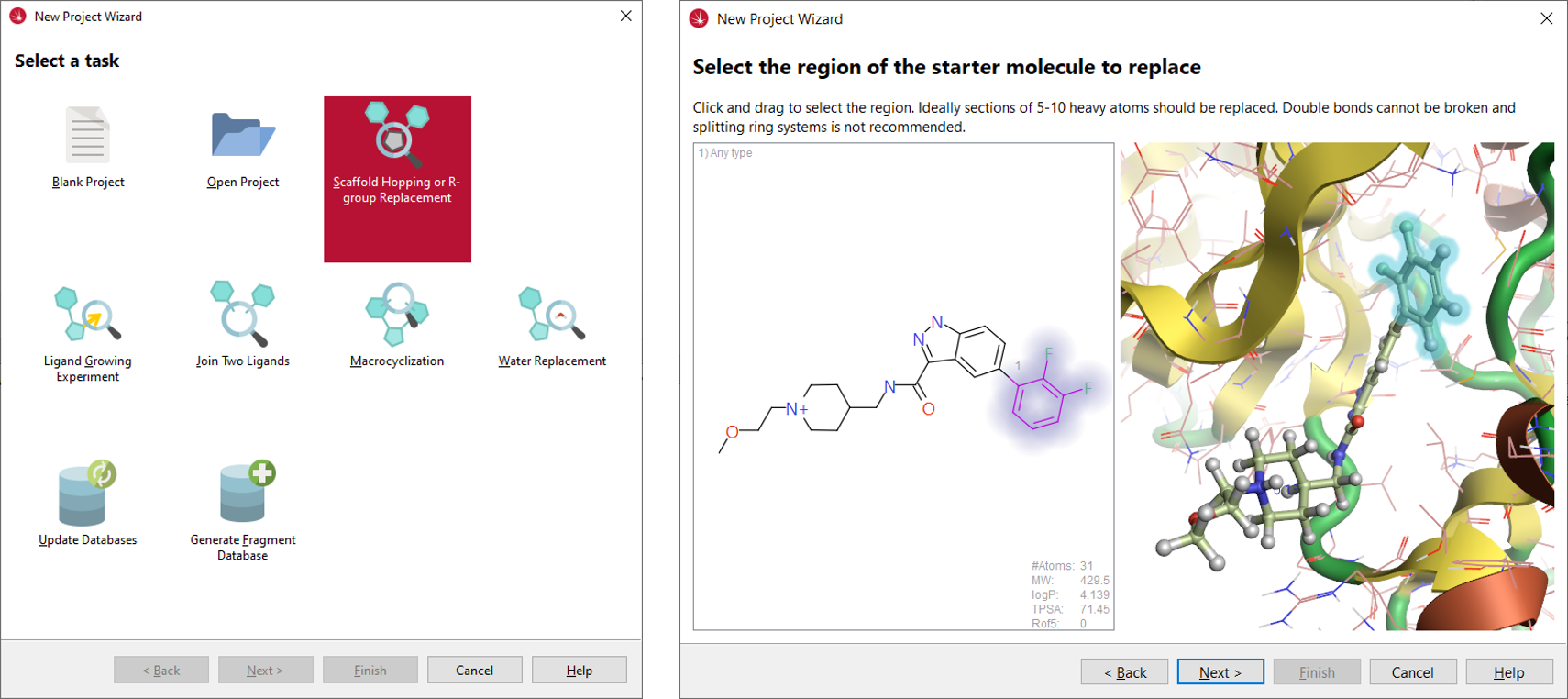
図4. 左: Sparkの新しいプロジェクトウィザード 右: Sparkウィザードで、出発分子の置換選択領域がハイライトされる
ウィザード操作を完了すると、Sparkの計算方法が「ドッキング」に自動的に設定されます。 この方法は、リガンドの類似性に基づく従来のSpark探索よりも計算量が多いため、適切な物理化学的フィルタを設定して探索空間を制限し、計算時間を短縮して目的に見合う実験を行うことが推奨されます。ここでは、出発分子(MW 429.5、SlogP 4.1)の特徴をガイドとして、結果分子の分子量を466未満、SlogPを3.5未満に設定しました。また、適切なSMARTSフィルタを使用して、置換フェニル基と2-ヒドロキシピリジンを結果から排除するようフィルタで除外しました(図5)。
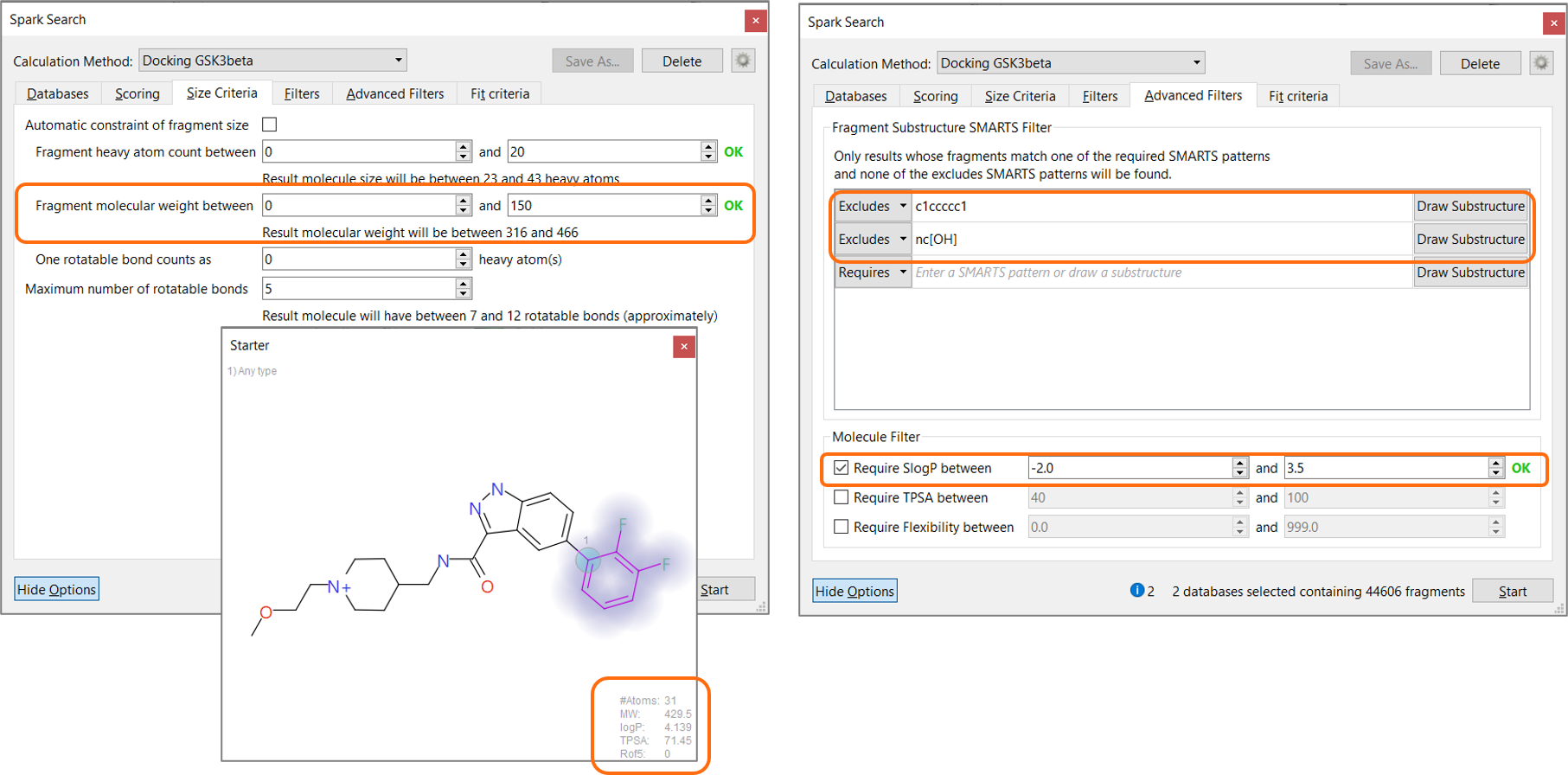
図5. 適切な物理化学的フィルタの設定による計算時間短縮と合目的的探索
実験は、eMoleculesビルディングブロック4に由来する約4,500個の芳香族ボロン酸と約40,000個の芳香族ハロゲン化物のデータベースを用いて実行され、論文に掲げられた化学を可能な限り再現しました2。
結果
Sparkのドッキングの結果、ランキング上位のいくつかのクラスタ(図6、左)の中に、ピリジン-3-イル置換基が見つかりました。またそのクラスタメンバの中は、表1で報告されたものと同一または類似のR-基(図6-中央)が多く含まれていることがわかります。さらに、他の上位のクラスタでは、分子量と親油性が低く抑えられたさまざまな二環式複素環も見つかります。これはリードシリーズの探索を進めていく上で、ピリジン-3-イル置換基に対する興味深い代替置換基となる可能性があります。いくつかの例を図6右に示します。
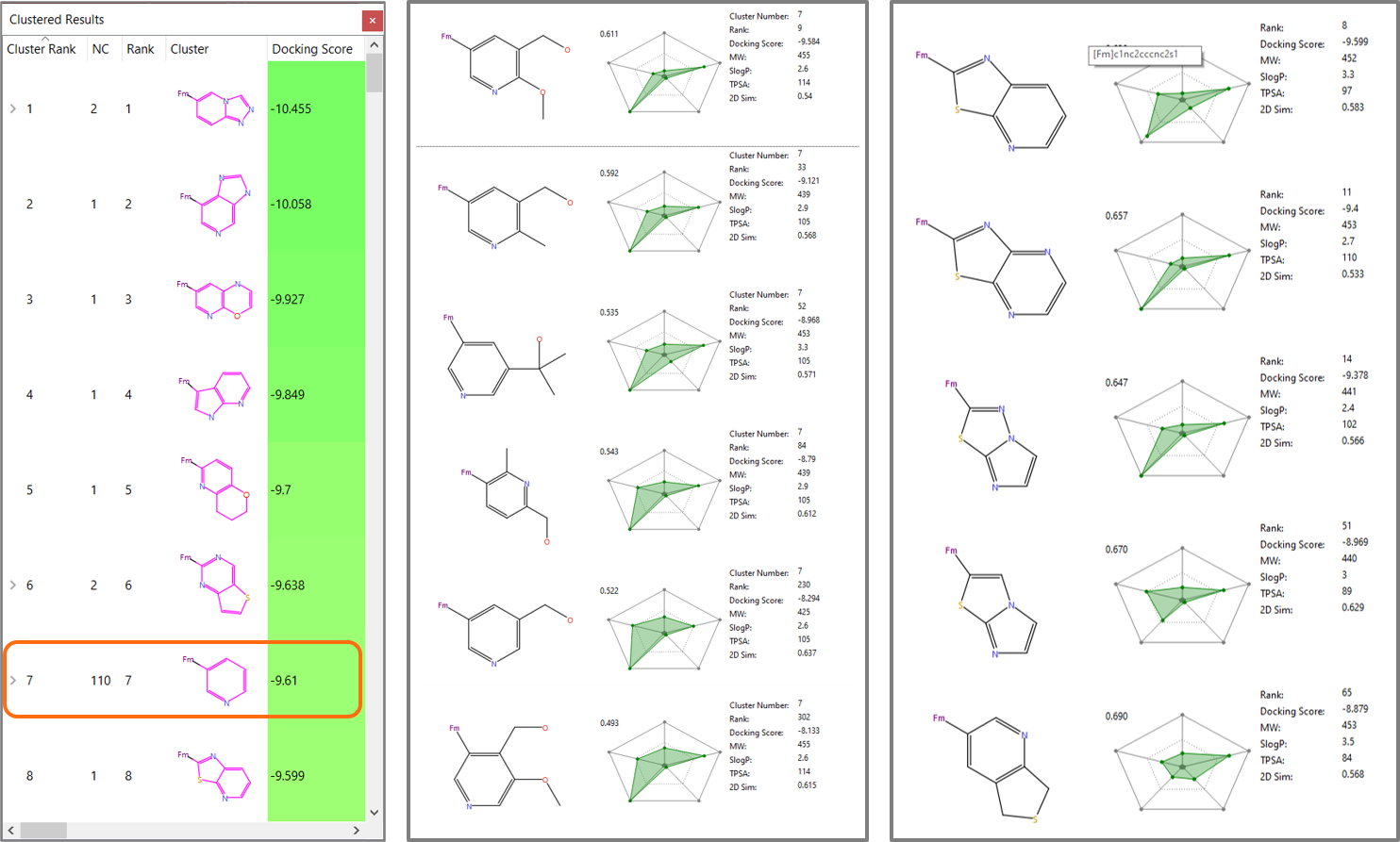
図6. 左: ピリジン-3-イル置換基2のクラスタランクは7位 中央: そのクラスタのメンバは表1に類似する置換基を多く含む 右:分子量と親油性が低く抑えられた二環式複素環
興味深いことに、Sparkがピリジン-3-イルクラスタの多くのメンバに対して示唆された結合モードには、Lys85との水素結合、場合によってはPhe67とのπ-π相互作用が含まれ、化合物OH84 (PDB: 6Y9R、図7) の結晶学的結合モードと一致します。 当然のことながらドッキング法では、残基との水素結合を追加することのできる置換基(ヒドロキシルなど)をもつ3-ピリジンを優先する傾向があり、その場合には、活性部位にあるAsp200などがそれを実際に可能にします。
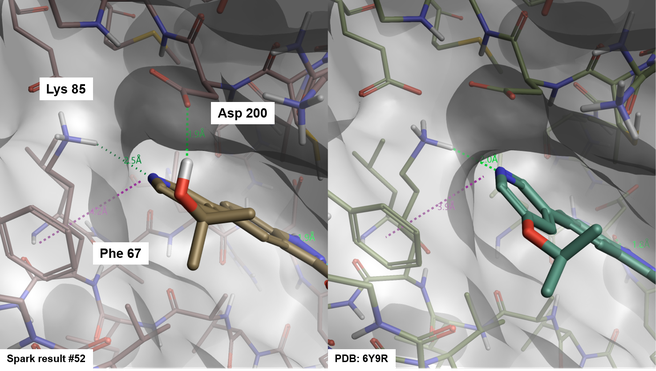
図7. Spark結果 #52(左)とPDBからの化合物OH8の結合モード(6Y9R、右)
結論
「ドッキング」機能により、Sparkはタンパク質活性部位から直接リガンド-蛋白質相互作用を可能にするフラグメントを見つけることができます。 この方法を利用すると、リガンドとフラグメントを標的タンパク質内の活性ポケットの空隙に成長させ、既存の出発分子またはレファレンス分子にはなかった相互作用をする新しい分子を発見することもできます。
参考文献
1. Ombrato R. et al., J. Chem. Inf. Model. 2015, 55, 2540−2551
2. Prati F. et al., ACS Med. Chem. Lett. 2020, 11, 825−831
3. Buonfiglio R. et al., Molecules 2020, 25(9), 2163
4. https://www.emolecules.com/info/products-building-blocks.html