Improving PROTAC properties via single-point changes to linkers
We explore how computational methods can be applied to proteolysis targeting chimera (PROTAC) design, to effectively tackle some of the ...
News
Spark™V10.6は、スキャフォールドホッピングや生物学的等価体(Bioisostere)置換ツールの新しいバージョンとしてリリースされました。様々な創薬プロジェクトにおいて創薬/計算化学者が本リリースの新しい機能と改善された分子探索方法を利用し、一層革新的なアイデアを創出することができるよう支援します。
Sparkの新規「ドッキング」機能により、タンパク質活性部位から直接リガンド-蛋白相互作用と符合するフラグメントを見つけることができます。リガンドとフラグメントをターゲットタンパク質のポケット内の空隙に成長させ、出発分子や参照分子になかったタンパク質との相互作用を伴って部分置換された新たな分子を発生します。
図1にこの新しいワークフローの詳細を示します。 Sparkは出発分子の置換部分を削除することから始めます(図1、A-B)。次に、一部を切り取られた出発分子に新しいフラグメントを加え、Cresset XED力場によって計算されるタンパク質の静電場に従ってその活性部位に適切に配置します(図1、C)。そしてLeadFinder™の「スコアリング」ドッキングモードを使用して、新しい結果分子のポーズを最適化します(図1、D)。最後に、既知のリガンドの結晶学的ポーズを正しく評価するよう最適化されたLeadFinderの「ランク」スコアリング関数を使用して、得られた複数のポーズの優先順位を決定します。
また、リガンド-蛋白相互作用のドッキング制約を設定すれば、その制約を重視する結果分子を簡単に得ることができます。
Sparkのドッキングは、従来のbioisostere置換方法に追加するアドオンとして提供されます。ご興味のある方は弊社までご連絡ください(連絡先l)。
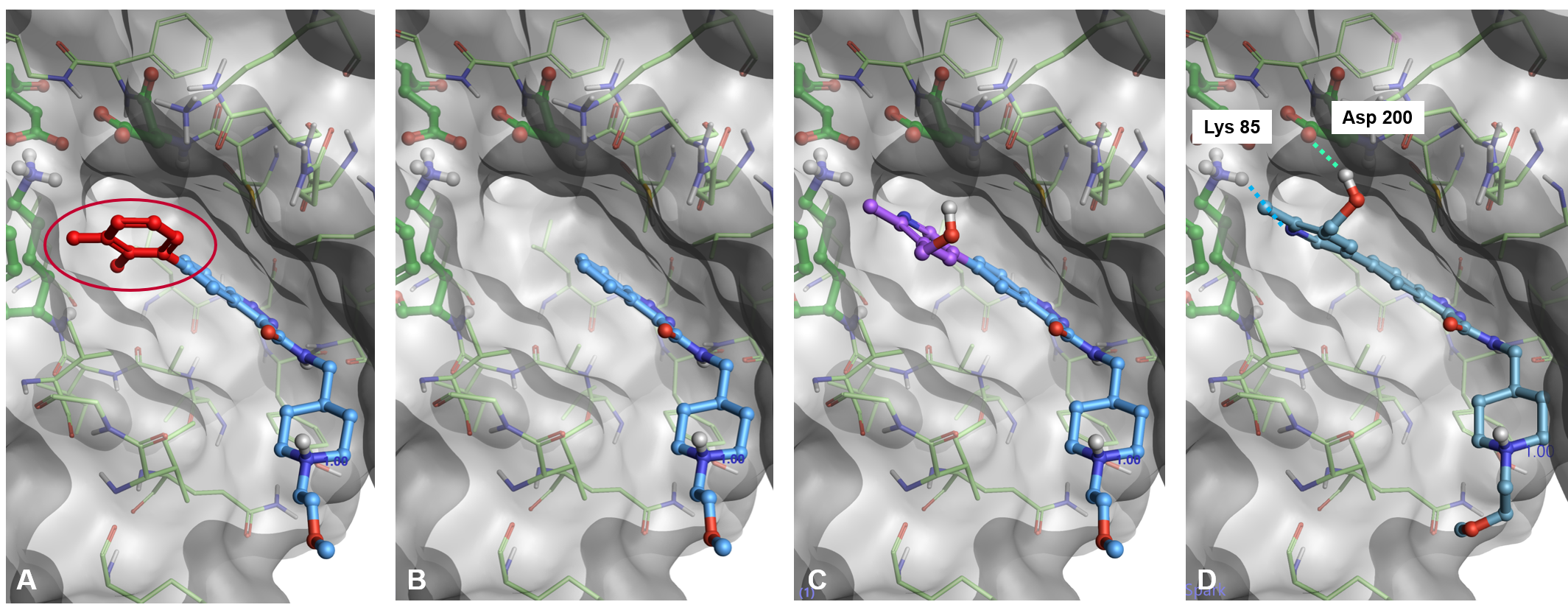
図1: Sparkでのドッキングワークフロー(PDB: 6TCU) A) 出発分子の置換部分の選択 B) 選択フラグメントの削除 C) 新しいフラグメントポケットの中で適切に結合 D) 新規結果分子をLeadFinderで最適化
リガンドのField/Shape類似性に基づくSparkの従来法も以下に示す改善がなされました。
これらの改善によって、興味深いbioisostereを見つけるSparkの探索精度が向上します。例えば、鉱質コルチコイド受容体調整薬のX線構造(PDB: 5MWP)のリガンドのスキャフォールドホッピング実験で、他の既知の鉱質コルチコイドリガンドによく似た構造がいくつも見つかります(図2)。結果リストを見れば、高いbioisoster係数(BIF%)をもつ分子が濃縮されていることがわかります。これらの改善により、通常のR-グループ置換実験で、高いBIF%をもつ結果分子が30%ほど多く得られます。
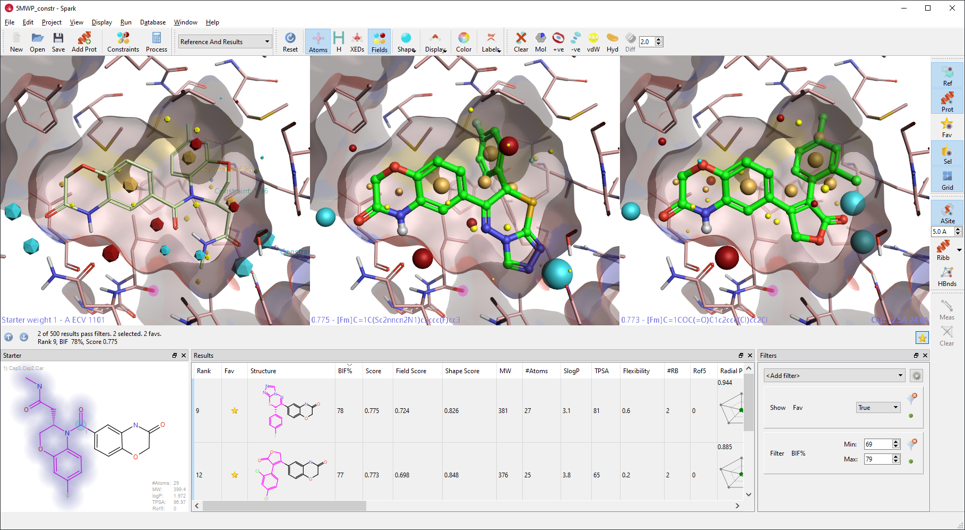
図2: 5MWPのスキャフォールドホッピング実験。鉱質コルチコイド受容体の既知のスキャフォールドに対して高いBIF%をもつスキャフォールドが見いだされる
探索中に適切なフィルターを設定しSparkの探索空間を狭めることは、計算時間を短縮するばかりでなく、よりよい結果を得るために重要な鍵となります。フラグメント成長実験やドッキング探索を行う際に適切な制限を設けることはとても効果的です。
高度なSpark探索オプション(図3)の[サイズ基準]パネルが改善されました。これにより、フラグメントと結果分子の両方の重原子の数、MW、および回転可能な結合の数が表示されます。このパネルを出発分子ウィンドーおよび高度フィルターの情報と組み合わせて使用して、理想的な物理化学的プロファイルをもつ分子群がSpark実験によって得られます。
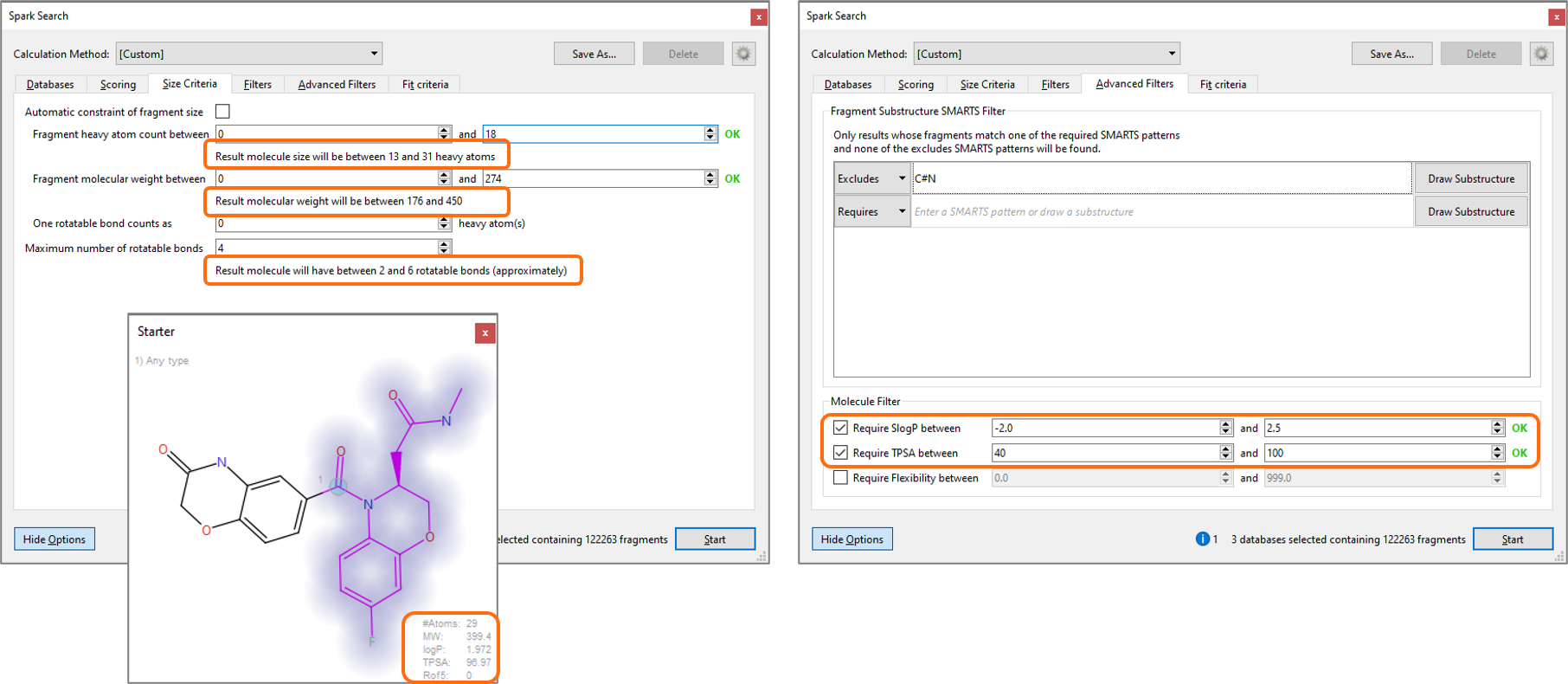
図3: 改善されたサイズ基準パネル(左)、出発分子ウィンドー(下)および高度フィルター(右)の情報を合わせて適切な物理化学的プロファイルをもつ結果分子を設定
このSparkV10.6リリースは、下に示すようなユーザーインターフェイスの大幅な改善とともに、新しい科学を提供します。
現在のSparkのお客様へはすでに、SparkV10.6への更新方法が詳細に説明された電子メールをお送りしてあります。
はじめてプロジェクトで試してみたい方は、ぜひ一度評価リクエスト をお送りください。